بررسی نقش PRF (Platelet-Rich Fibrin) در موفقیت درمان ایمپلنت
در دنیای مدرن دندانپزشکی، موفقیت ایمپلنت ها تنها به مهارت جراحی یا کیفیت ایمپلنت بستگی ندارد. کیفیت بافت های اطراف، سرعت بهبود استخوان و سلامت لثه، نقش بسیار مهمی در طول عمر و عملکرد ایمپلنت دارند. یکی از ابزارهای جدید و کم تهاجمی که در سال های اخیر مورد توجه قرار گرفته، PRF یا Platelet-Rich Fibrin است. در بسیاری از پروتکل ها این روش به عنوان PRF در ایمپلنت طبقه بندی می شود.
تعریف PRF
PRF یا Platelet-Rich Fibrin یک کنسانتره طبیعی از پلاکت ها و فیبرین است که از خون خود بیمار بدون هیچ ماده افزودنی شیمیایی تهیه می شود. این محصول بیولوژیک در فرآیند سانتریفیوژ، به صورت یک شبکه فیبرینی سه بعدی تشکیل می شود که داخل آن مقادیر بالایی از فاکتورهای رشد، سایتوکاین ها و سلول های التهابی مفید (مثل لکوکیت ها) ذخیره شده است. این فاکتورهای رشد به صورت تدریجی و کنترل شده در محل جراحی آزاد می شوند و همین ویژگی باعث تسریع و تقویت چند فرآیند اصلی می شود:
- افزایش نئوواسکولاریزاسیون (رشد عروق جدید)
- تحریک سلول های استخوان ساز (استئوبلاست ها)
- بهبود ترمیم بافت نرم و کاهش التهاب
- شکل گیری سریع تر لخته پایدار و کیفیت بهتر زخم
به همین دلیل در درمان های ایمپلنت، PRF نه به عنوان “جایگزین” استخوان یا گرافت، بلکه به عنوان یک کمک کننده بیولوژیک تقویت کننده استفاده می شود؛ یعنی حضور آن باعث می شود روند ترمیم سریع تر، پایدارتر و با پیش بینی پذیری بالاتر پیش برود. مطالعات جدید نشان داده اند که استفاده از PRF در ایمپلنت می تواند احتمال موفقیت طولانی مدت ایمپلنت ها را افزایش دهد، تحلیل بافتی را کاهش دهد و کیفیت استخوان و لثه اطراف ایمپلنت را بهبود بخشد. به طور خلاصه PRF بدن را وادار می کند به شکل طبیعی تر، سریع تر و با کیفیت بالاتر التیام یابد. در این مقاله، به بررسی نقش PRF در ایمپلنت در:
- افزایش ثبات ایمپلنت
- بهبود بافت نرم اطراف ایمپلنت
- تقویت استخوان و کمک به گرافت ها
می پردازیم و شواهد علمی جدید را بررسی می کنیم. این موضوع در نواحی با تراکم استخوانی ضعیف در فک انسان و موقعیت هایی که تعداد ایمپلنت فک محدود است، اهمیت بیشتری دارد.
تعریف و نحوه اثر انواع PRF
در این بخش به طور دقیق به تعریف انواع prf می پردازیم و سپس در خصوص نحوه اثر آن به طور مفصل توضیحاتی را بیان خواهیم کرد:
تعریف انواع PRF
PRF یک نوع ماتریس پلاکتی خودی (autologous) است که برخلاف PRP، نیازی به افزودن مواد شیمیایی یا فعال کننده ندارد. این ماده طبیعی، سرشار از فاکتورهای رشد است و با ساختار فیبرینی خود محیطی مناسب برای رشد سلول ها فراهم می کند و به خصوص زمانی که قرار است روکش ایمپلنت در فاز سریع تر تحویل شود، از لحاظ بیولوژیک حمایت گر محسوب می شود و در این پروتکل ها نیز به عنوان PRF در ایمپلنت یاد می شود. نسل های مختلف PRF شامل:
- L-PRF
- A-PRF
- i-PRF
- e-PRF
هستند که هر کدام روش آماده سازی و سرعت سانتریفیوژ متفاوتی دارند و به همین دلیل میزان فاکتورهای رشد و سلول های موجود در آن ها کمی متفاوت است.
نحوه اثر PRF
PRF با فراهم کردن یک محیط بیولوژیک فعال و کنترل شده، روند ترمیم بافت را از چند جهت تقویت می کند. مهم ترین مکانیسم های اثر آن شامل موارد زیر است:
1. افزایش تکثیر و فعالیت سلولی
PRF حاوی فاکتورهای رشد کلیدی مثل PDGF ،TGF-β و VEGF است. این فاکتورها سلول های استخوان ساز (استئوبلاست ها)، سلول های بافت نرم و سلول های اندوتلیال را تحریک می کنند و به این ترتیب روند بازسازی استخوان، تشکیل عروق جدید و ترمیم بافت نرم سرعت بیشتری پیدا می کند. این مکانیزم یکی از دلایل تأثیرگذاری PRF در ایمپلنت محسوب می شود و در کیس هایی که مراحل قالب گیری ایمپلنت نیاز به پایداری لثه دارد، کارایی آن بیشتر دیده می شود.
2. تشکیل یک داربست فیبرینی با ثبات بالا
شبکه فیبرین متراکم در PRF مانند یک داربست طبیعی عمل می کند. این داربست به سلول های ترمیمی فضای مناسب برای چسبیدن، مهاجرت و تکثیر می دهد. این موضوع باعث می شود لخته پایدارتر باقی بماند و محیط اولیه زخم به صورت سازمان یافته تری به سمت ترمیم پیش برود. این اثر در بسیاری از پروتکل های PRF در ایمپلنت برای افزایش پایداری محیط جراحی مورد توجه قرار گرفته است.
3. کنترل التهاب و بهبود کیفیت ترمیم
وجود لکوسیت ها و سایتوکاین های تنظیم کننده التهاب در PRF کمک می کند پاسخ التهابی بیش از حد رخ ندهد؛ اما التهاب مفید اولیه برای شروع روند ترمیم حفظ شود. نتیجه آن، ترمیم سریع تر، کاهش درد، و کیفیت بهتر بافت نهایی است.
نحوه آماده سازی PRF
آماده کردن PRF معمولاً در سه مرحله انجام می شود:
- گرفتن خون از بیمار: حدود ۱۰ تا ۲۰ میلی لیتر خون از ورید گرفته می شود و داخل لوله های مخصوص قرار می گیرد. نکته مهم این است که داخل لوله ها هیچ ماده ضدانعقاد وجود ندارد که همین موضوع تفاوت اصلی با PRP است.
- سانتریفیوژ کردن: بلافاصله بعد از خون گیری، لوله ها داخل سانتریفیوژ قرار می گیرند. سرعت و زمان چرخش، بسته به نوع PRF (مثل L-PRF یا A-PRF یا i-PRF) متفاوت است. به عنوان مثال برای L-PRF معمولاً حدود ۲۷۰۰ دور در دقیقه حدود ۱۲ دقیقه رایج است. البته هر دستگاه پروتکل خودش را دارد و عددها دقیقاً مثل هم نیستند.
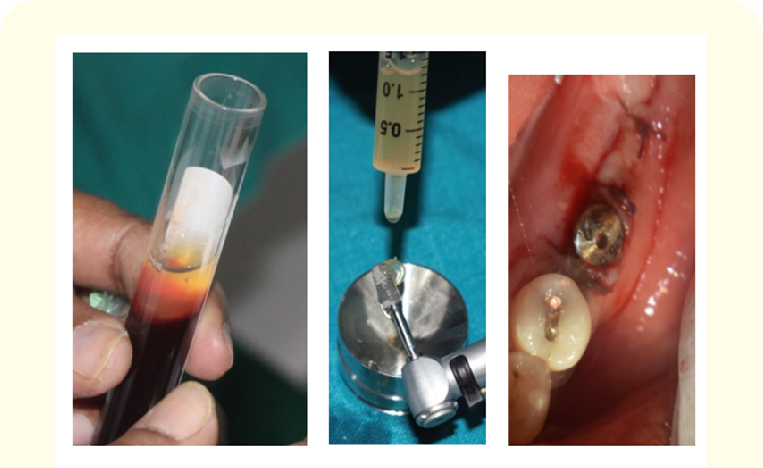
- جداسازی و استفاده از لایه PRF:بعد از چرخش، خون به ۳ لایه تقسیم می شود:
• پایین: گلبول های قرمز
• وسط: لایه فیبرینی زرد رنگ (همان PRF اصلی)
• بالا: پلاسما
لایه وسط جدا می شود و بسته به نیاز جراح، یا به شکل غشاء استفاده می شود، یا با پودر استخوان مخلوط می شود.
نکته مهم برای کلینیک ها: برای اینکه نتیجه ها همیشه قابل پیش بینی و یکسان باشد، باید سرعت و زمان سانتریفیوژ دقیق و ثابت باشد. حتی تغییر چند صد rpm می تواند مقدار فاکتورهای رشد داخل PRF را کم و زیاد کند. به همین دلیل کلینیک ها معمولاً سانتریفیوژ اختصاصی PRF تهیه می کنند و از سانتریفیوژهای عمومی آزمایشگاهی استفاده نمی کنند.
نقش PRF در تثبیت و موفقیت ایمپلنت
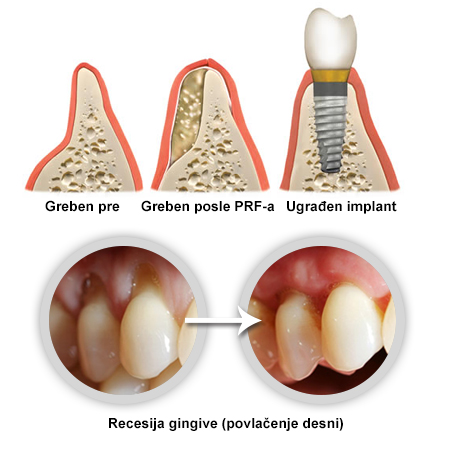
وقتی ایمپلنت قرار داده می شود، ثبات اولیه بیشتر یک مسئله مکانیکی است: یعنی تماس مستقیم رزوه های ایمپلنت با استخوان. اما نتیجه نهایی درمان به ثبات ثانویه وابسته است؛ یعنی زمانی که استخوان جدید اطراف ایمپلنت ساخته و یکپارچه می شود (osseointegration). این مرحله دقیقاً همان مرحله ای است که در بسیاری از پروتکل های جدید PRF در ایمپلنت بیشترین توجه را به خود جلب کرده است. PRF در این مرحله می تواند نقش بسیار مهمی داشته باشد:
- با آزادسازی تدریجی فاکتورهای رشد، سلول های استخوانی را فعال می کند.
- با ایجاد داربست فیبرینی، شرایط میکروبیولوژیک محل ایمپلنت برای تشکیل استخوان جدید مساعدتر می شود.
- التهاب اضافه را کنترل می کند و اجازه می دهد بازسازی به صورت منظم و پایدار اتفاق بیفتد.
در نتیجه، PRF نه به عنوان جایگزین مواد گرافت یا تکنیک جراحی، بلکه به عنوان تقویت کننده بیولوژیک نتایج عمل می کند و می تواند کیفیت و سرعت شکل گیری ثبات ثانویه را بهبود دهد. این بخش مهمی از پروتکل های نوین PRF در ایمپلنت است.
این موضوع در کیس هایی که نیاز به افزایش حجم استخوان، سینوس لیفت یا ترمیم بافت نرم دارند، اهمیت دوچندان پیدا می کند، خصوصاً زمانی که با نیروی دقیق و برنامه ریزیشده موتور ایمپلنت و تورک کنترل شده همزمان استفاده شود، تا پایداری اولیه و شرایط فیزیولوژیک محیط بهتر کنترل شود.
شواهد علمی
- مطالعات نشان می دهند که استفاده از PRF در ایمپلنت موجب افزایش میزان ISQ (شاخص ثبات ایمپلنت) در فازهای بعدی می شود.
- ایمپلنت هایی که با PRF پوشانده می شوند، معمولاً سرعت بهبود استخوان اطراف و تثبیت ثانویه بیشتری دارند.
- PRF همچنین می تواند در شرایط خاص مانند استخوان کم کیفیت یا ایمپلنت های فوری، التهاب را کاهش دهد و روند بهبود را سریع تر کند.
نکات مهم در استفاده از PRF
- اثرات PRF اغلب در کوتاه مدت مشاهده می شوند و مطالعات بلندمدت هنوز محدود هستند.
- روش آماده سازی PRF بین مطالعات متفاوت است و همین امر می تواند نتایج را متفاوت نشان دهد.
- تاثیر بالینی آن ممکن است در بعضی موارد کوچک باشد، بنابراین نباید به عنوان جایگزین کامل تکنیک های استاندارد درمان ایمپلنت در نظر گرفته شود.
تاثیر PRF بر بهبود بافت نرم اطراف ایمپلنت
سلامت لثه و مخاط اطراف ایمپلنت فقط مسئله زیبایی نیست؛ بلکه یک عامل تعیین کننده در ثبات و پیش بینی پذیری بلندمدت ایمپلنت محسوب می شود. وقتی عرض مناسب لثه کراتینه و ضخامت کافی بافت نرم وجود داشته باشد، یک seal بیولوژیک پایدار اطراف ایمپلنت شکل می گیرد که از ورود میکروب ها، التهاب مزمن و تحلیل استخوان جلوگیری می کند. در مقابل، ناپایداری بافت نرم می تواند مسیر ایجاد میوکوزیت و در نهایت پری ایمپلانتایتیس را فراهم کند. بنابراین تقویت کیفیت بافت نرم، یک مؤلفه اساسی در موفقیت درمان ایمپلنت است و نه یک گزینه فرعی. این بخش نیز از بخش های مهم پروتکل های امروزی PRF در ایمپلنت است.
نحوه کمک کردن PRF
PRF از خون خود بیمار به دست میآید و این مزیت باعث می شود کاملاً سازگار زیستی باشد و بدون ریسک واکنش حساسیتی عمل کند. نقش آن در بهبود بافت نرم به چند مکانیزم اصلی مرتبط است:
- تقویت ضخامت و کیفیت مخاط: قرار دادن غشاء PRF روی لثه منبعی از فاکتورهای رشد فراهم می کند که سلول های اپی تلیال و فیبروبلاست ها را تحریک می کند و در نتیجه ضخامت و استحکام بافت نرم افزایش می یابد. این امر در نواحی که لثه نازک است، اهمیت بیشتری پیدا می کند و در همین شرایط استفاده از PRF در ایمپلنت می تواند منجر به ثبات بلند مدت بهتر شود.
- کاهش التهاب و درد پس از جراحی: PRF فاکتورهای رشد را به صورت تدریجی آزاد می کند و این باعث می شود التهاب کنترل شده، لخته پایدارتر تشکیل شود و ترمیم زخم با سرعت طبیعی تر پیش برود. بیماران معمولاً تجربه درد و حساسیت کمتری دارند.
- کم تهاجمی بودن نسبت به گرافت کلاسیک: در برخی کیس ها می توان از PRF به عنوان جایگزین نسبی پیوند بافت نرم استفاده کرد، بدون اینکه نیاز باشد از کام بیمار بافت برداشت شود. این موضوع زمان جراحی را کوتاه تر و احتمال عوارض ناحیه برداشت را کمتر می کند.
کاربرد PRF در تقویت استخوان و گرافت ها

در این بخش در خصوص کاربرد prf ها در تقویت استخوان ها و گرافت ها به تفصیل توضیحاتی داده شده است.
نقش PRF در گرافت استخوانی
در مواردی که برای قرار دادن ایمپلنت نیاز به افزایش حجم استخوان وجود دارد، PRF به عنوان یک تقویت کننده بیولوژیک در کنار مواد گرافت مورد استفاده قرار می گیرد. حضور فاکتورهای رشد و ساختار فیبرینی PRF باعث می شود محیط محل جراحی از نظر سلولی و عروقی فعال تر شود و روند تشکیل استخوان جدید سریع تر و قابل پیش بینی تر پیش برود. بسیاری از مواد گرافت استخوانی در کیس های PRF در ایمپلنت به علت همین مزیت ترکیب می شوند.
با ایجاد محیط مناسب برای رشد سلول های استخوان ساز، فرایند استئواوینگرشن تسریع می شود و استخوان تازه با کیفیت بیشتری تشکیل می شود. مطالعات نشان می دهند ترکیب PRF با گرافت های استخوانی، علاوه بر بهبود حجم، در حفظ ارتفاع و جلوگیری از تحلیل عمودی استخوان موثر واقع شود و به تثبیت بهتر ایمپلنت در درازمدت کمک کند.
در واقع PRF به تنهایی نقش “جایگزین استخوان” ندارد، اما کیفیت ترمیم استخوان را به شکل معنی داری ارتقا می دهد و همین ارتقا، یکی از دلایل محبوبیت PRF در ایمپلنت در سال های اخیر بوده است.
استفاده از PRF در سینوس لیفت
در پروسیجر سینوس لیفت، خصوصاً در کیس های با نقص خفیف تا متوسط، افزودن PRF به مواد گرافت باعث بهبود روند بازسازی و افزایش کیفیت استخوان می شود. ترکیب PRF با گرافت در سینوس لیفت، عروق سازی را تقویت می کند و این موضوع برای پایداری استخوان جدید در فضای سینوس اهمیت زیادی دارد.
PRF می تواند به شکل غشاء روی گرافت قرار گیرد یا به صورت ترکیب شده داخل ماده استخوانی استفاده شود و در هر دو حالت فرایند بازسازی استخوان را تسریع می کند. این ویژگی باعث شده بسیاری از جراحان امروزه PRF در ایمپلنت را به عنوان یک بخش استاندارد در سینوس لیفت های محدود در نظر بگیرند.
محدودیت ها و نکات واقع گرایانه
PRF به تنهایی نمی تواند جایگزین کامل گرافت های بزرگ یا نقصهای حجمی شدید شود؛ بلکه نقش آن بیشتر افزاینده و تسریع کننده ترمیم است.
نتایج مطالعات به نوع PRF، سرعت و پروتکل سانتریفیوژ و نسل مورد استفاده (L-PRF ،A-PRF و …) وابسته است؛ بنابراین استاندارد سازی روش تهیه PRF در کلینیک مهم است تا نتایج قابل تکرار و پیش بینی پذیر باقی بمانند.
جمع بندی و نتیجه گیری
استفاده از PRF در درمان ایمپلنت ها می تواند ثبات ثانویه ایمپلنت را افزایش دهد و ضخامت و کیفیت بافت نرم پیرامون ایمپلنت را بهبود بخشد. همچنین PRF می تواند در ترکیب با گرافت استخوانی یا سینوس لیفت، روند بازسازی استخوان را تقویت کند. با این حال شواهد بلندمدت محدود است و بیشتر مطالعات کوتاه مدت هستند و پروتکل های آماده سازی PRF متنوع هستند و اثر بالینی آن در برخی موارد کوچک است.
نتیجه عملی برای دندانپزشکان:
- PRF را می توان به عنوان یک مکمل کم ریسک در موارد پرریسک استفاده کرد.
- ترکیب PRF با گرافت یا غشاء ممبرن، بهترین نتیجه را ارائه می دهد.
- اطلاع رسانی به بیمار درباره مزایا و محدودیت ها ضروری است.
- ثبت نتایج و پیگیری طولانی مدت، تجربه بالینی شما را بهبود می بخشد.
PRF یک ابزار کمکی مطمئن و رو به رشد است که می تواند به موفقیت طولانی مدت ایمپلنت ها کمک کند، اما هنوز نمی توان آن را جایگزین استانداردهای درمانی اصلی دانست. مطالعات آینده با طراحی دقیق و استانداردسازی روش ها، نقش واقعی PRF در ایمپلنت ها را روشن خواهند کرد.











